Раздел IV.
МЕТАЛЛУРГИЧЕСКИЕ ОСНОВЫ СВАРКИ ПЛАВЛЕНИЕМ
НАЗАД:
4.2.4. Влияние водорода на свойства
металлов
4.3. Шлаковая фаза при сварке плавлением
Шлаком называется
неметаллический покров на поверхности металла шва. Он образуется за счет
плавления электродного покрытия, флюса, шихты порошковой проволоки или за счет
металлургических процессов, протекающих при сварке (например, при сварке в
углекислом газе).
Назначение шлака – получить
желаемое направление процессов при сварке, а именно:
-
защитить
расплавленный металл от взаимодействия с газовой фазой;
-
обеспечить
необходимые сварочно-технологические свойства процесса: минимальное
разбрызгивание, хорошее формирование шва, стабильное существование дугового
разряда, газовыделение из металла шва, легкую отделимость шлаковой корки от
поверхности закристаллизовавшегося металла шва;
-
обеспечить
протекание требуемых металлургических процессов в зоне плавления – раскисления,
легирования, рафинирования, связывания водорода в соединения, нерастворимые в
металле;
-
замедлить
остывание металла шва после сварки.
По своему составу шлаки
представляют сложную систему из оксидов и (или) нейтральных солей, между
которыми могут происходить химические реакции, приводящие к образованию новых
веществ. Главные шлаковые компоненты, применяемые в сварочных шлаках, можно
разбить на четыре группы (табл. 9).
Таблица 9. Главные
компоненты сварочных шлаков
|
Кислотные оксиды |
Основные оксиды |
Амфотерные оксиды |
Нейтральные соли |
|
SiO2, TiO2, B2O3, P2O5,
ZrO2 |
Na2O, K2O, CaO, MgO, FeO, MnO |
Al2O3, Fe2O3, Cr2O3,
V2O3 |
KF, NaF, LiF, CaF2, BaF2, KCl, NaCl, MgCl2,
Na3AlF6 (криолит) |
В расплавленном состоянии
основные оксиды взаимодействуют с кислотными или амфотерными и образуют
химические соединения – комплексные оксиды, как правило, более жидкотекучие и
легкоплавкие. Например:
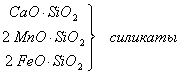
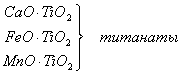
![]()
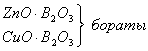
В настоящее время
существуют две теории, описывающие строение жидких шлаков – молекулярная и
ионная [14]. Наиболее
распространенной теорией строения жидких шлаков явилась молекулярная теория,
развитая в основном Г. Шенком. В соответствии с молекулярной теорией, шлаки –
это системы свободных и химически связанных неметаллических соединений (оксидов
и пр.), между которыми имеется подвижное химическое равновесие. При этом с
металлом взаимодействуют только свободные компоненты (в частности оксиды).
Более поздняя – ионная
теория предполагает, что шлаки имеют строение ионного типа. В соответствии с
этой теорией в жидких шлаках все оксиды и их химические соединения
диссоциированы на ионы. В расплавленных шлаках находятся положительно заряженные
катионы Ca2+, Mg2+, Mn2+, Al3+ и др. и
отрицательно заряженные анионы O2-, F-, S2-, SiO![]() , TiO
, TiO![]() и др. Наибольший вклад
в теорию электрохимии металлургических шлаков внесла школа О.А. Есина.
и др. Наибольший вклад
в теорию электрохимии металлургических шлаков внесла школа О.А. Есина.
Молекулярная теория шлаков
разработана достаточно детально, более удобна для практических расчетов
равновесных систем. Поэтому в большинстве сварочной литературы сварочные шлаки
рассматриваются как молекулярные растворы.
Важнейшие показатели
хорошего сварочного шлака – его способность связывать оксиды, нитриды,
сульфиды, фосфиды в прочные химические соединения, нерастворимые в металле и
легко удаляемые в шлак.
Характер протекания
металлургических процессов между металлом и шлаком зависит от химического
состава шлака. Формально преобладание кислотных или основных характеристик
шлака оценивается коэффициентом основности В или кислотности К:
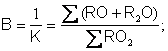 (4.17)
(4.17)
где SRO2 –
суммарное содержание (%) кислотных оксидов в шлаке;
S(RO+R2O) – суммарное
содержание (%) основных оксидов в шлаке.
С учетом активности каждого
из компонентов шлака коэффициент основности имеет следующий вид [13]:
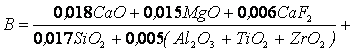
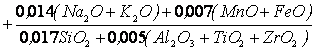 ; (4.18)
; (4.18)
где CaO, MgO и т.д. – массовые доли соответствующих компонентов в
шлаке, %.
Если В > 1, то шлак считается основным, если В < 1 – кислым, при В = 1 – нейтральным.
Обычно в сварочных шлаках В
= 0,6 ¸ 1,3, но уже при В > 1,1 ухудшаются сварочно-технологические свойства
шлака.
Кислый шлак хорошо
раскисляет стали за счет связывания FeO в
комплексные соединения с SiO2, TiO2. Но большие скорости охлаждения не позволяют довести
процесс до конца. Приходится применять и раскислители. Но кислый шлак не может
рафинировать металл. Поэтому сырые (т.е. исходные) материалы должны иметь
минимальное содержание серы и фосфора (не более 0,10 % каждого).
Основные шлаки не могут
связать FeO в комплексы. Поэтому требуют большего количества
раскислителей. Но они хорошо связывают серу и фосфор в комплексные соединения,
удаляемые в шлак.
Шлак должен обладать
следующими физическими свойствами:
·
температура
плавления шлака должна быть на 200 ¸ 300 0С ниже температуры плавления металла;
·
удельный вес
шлака должен быть меньше удельного веса металла;
·
шлак должен
обладать вязкостью на два порядка больше, чем металл (так, у сталей коэффициент
вязкости h = (1 ¸ 2)×10-3 Па.с, у шлаков - h = (0,8 ¸ 3)×10-1 Па.с);
·
сварочные шлаки
должны при расплавлении резко уменьшать свою вязкость, т.е. они должны быть
короткими (см. рис. 45);
·
шлаковая корка
должна легко отделяться от поверхности закристаллизовавшегося металла.
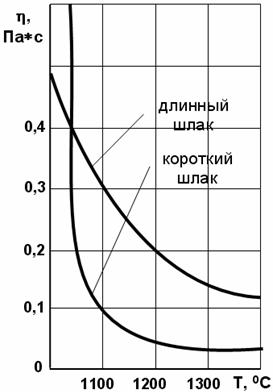
Рис. 45. Зависимость вязкости
шлаков от температуры:
1 – короткий шлак; 2 – длинный шлак
Шлаковая корка легко
удаляется при отсутствии шпинелей в шлаках. Шпинели - это комплексные
соединения типа MeR2O4, где в
качестве элемента Ме выступают Fe, Mn, Mg, а в качестве
элемента R – Al, Cr, V. Шпинель пристраивается к кристаллической решетке
стали, поэтому ее тяжело удалять с поверхности металла шва. Кроме того, для
хорошей отделимости шлака от металла шва необходимо, чтобы коэффициенты
линейного расширения металла и шлака a существенно отличались по своим величинам. Обычно у
сталей a×106 = 11,5 ¸ 14,0 1/0С, у шлаков a×108 = 9,9 ¸ 11,5 1/0С. Наилучшая отделяемость шлака
наблюдается при малой его окисленности.
Температура плавления и
удельный вес некоторых оксидов и соединений, образующихся при сварке сталей
приведен в табл. 10.
Таблица 10
|
Оксид или соединение |
Тпл, 0С |
g, г/см3 |
|
FeO |
1370 |
5,9 |
|
MnO |
1600 |
4,7 |
|
SiO2 |
1710 |
2,5 |
|
TiO2 |
1850 |
4,2 |
|
Al2O3 |
2050 |
3,9 |
|
CaO |
2570 |
3,4 |
|
2FeO×SiO2 |
1320 |
4,3 |
|
MnO×SiO2 |
1285 |
3,6 |
|
2MnO×SiO2 |
1365 |
4,1 |
|
FeS |
1193 |
4,6 |
|
MnS |
1620 |
4,0 |
Шлаки имеют три состояния:
жидкотекучее (h £ 1 Па×с), вязкое (h = 10 ¸ 102 Па×с) и хрупкое (h > 102 Па×с).
Те шлаки, у которых температурный интервал перехода из
вязкого состояния в жидкотекучее небольшой, называются короткими. Длинные шлаки
имеют значительно больший данный температурный интервал (см. рис. 45).
Короткие шлаки имеют вязкость почти постоянную в
интервале температур 1200 ¸ 1400 0С. При температуре около 1100 0С
вязкость коротких шлаков резко повышается и они затвердевают. Таким образом,
короткий шлак быстро затвердевает с поверхности, оставаясь жидким в зоне
соприкосновения с кристаллизующимся металлом. Это обеспечивает как свободный
выход газов из металла, так и соответствующее формирование шва. Короткие шлаки
– основные.
Длинные шлаки более густые,
их вязкость медленно снижается в интервале 1000 ¸ 1400 0С. Такие шлаки постепенно переходят
сначала из жидкого состояния в густое, потом – в тестообразное, а затем – в
твердое.
У длинных шлаков трудно
установить температуру начала их затвердевания. Переход из тестообразного
состояния в твердое у длинных шлаков сопровождается нарастанием вязкости, при
котором перегруппировка частиц, необходимая для получения кристаллической
решетки, затрудняется. Поэтому длинные шлаки не кристаллизуются, а переходят в
стекловидную массу.
Длинные шлаки – это обычно
кислые, силикатные шлаки. Чем больше содержание SiO2 в шлаке,
тем выше его вязкость. Длинные, густые, медленно затвердевающие шлаки менее
активны по отношению к металлу и отличаются худшими формирующими свойствами.
От вязкости шлака зависит его газопроницаемость, т.е.
способность пропускать выделяющиеся из металла газы. Скорость выделения газов
из металла зависит от их давления над поверхностью металла. Если у шлаков
плохая газопроницаемость, то на поверхности металла создается повышенное
давление газов, препятствующее их дальнейшему выделению. В этом случае в шве
может образоваться пористость, а на поверхности шва – мелкие вмятины, штриховатость,
побитость (см. рис. 46).
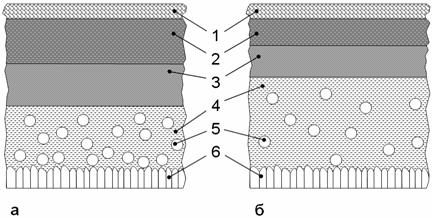
Рис. 46. Схема затвердевания длинного (а) и короткого
(б) шлаков:
1 – твердый шлак; 2 –
тестообразный шлак; 3 – густой шлак; 4 – жидкий шлак; 5 – газовые пузыри; 6 –
металл шва
Густые шлаки обладают плохой, а маловязкие подвижные
шлаки – высокой газопроницаемостью. В жидкотекучих шлаках быстрое выделение
газов из металла сопровождается попутным «захватом» частиц шлаковых включений и
более полным очищением металла шва. Поэтому важно правильно подбирать
соответствующие добавки к шлаку, чтобы влиять на его вязкость в нужном
направлении.
Лучшим разжижителем шлаков, особенно основных,
является фтористый кальций CaF2 (плавиковый шпат). Уменьшают вязкость также хлориды,
оксиды (TiO2, K2O, Na2O, MnO). Особенно благоприятно влияние TiO2, который
способствует получению короткого шлака.
Увеличивают вязкость SiO2, Al2O3, ZrO2, CaO, MgO.
Для сварки более желательны
маловязкие, легкоподвижные, быстро затвердевающие шлаки. Этому условию больше
всего удовлетворяют короткие, основные шлаки.
Главные шлаковые системы по
составу компонентов делятся на три типа: оксидные – силикаты и основные,
оксидно-солевые и солевые. Силикаты применяют для сварки малоуглеродистых и
низколегированных сталей, основные шлаковые системы – для сварки нержавеющих
высоколегированных сталей. Оксидно-солевые шлаки применяют для сварки средне- и
высоколегированных сталей и для наплавки, солевые – для сварки алюминиевых и
титановых сплавов.
По строению шлаки должны
иметь не более трех главных компонентов. Например, кислые электродные покрытия
построены на основе SiO2-FeO-MnO, основные на базе CaO-SiO2-CaF2, плавленые флюсы для сварки малоуглеродистых сталей
на основе SiO2-MnO-CaF2.
По содержанию двуокиси
кремния SiO2 и закиси
марганца MnO оксидные флюсы (шлаки)
разделяют на несколько категорий.
По содержанию SiO2:
- бескремнистые (SiO2
содержится в виде примесей в количестве не более 5 %);
- низкокремнистые
(содержание SiO2 = 6 ¸ 35 %);
- высококремнистые
(содержание SiO2 > 35 %).
По содержанию MnO:
- безмарганцовистые (MnO содержится в виде примесей не более 1 %);
- низкомарганцовистые
(содержание MnO до 10 %);
- среднемарганцовистые
(содержание MnO = 15 ¸ 30 %);
- высокомарганцовистые
(содержание MnO > 30 %).
Согласно рекомендации
Международного института сварки (МИС) сварочные флюсы по химическому
составу делятся на группы, приведенные в
табл. 11.
Таблица 11. Классификация
сварочных флюсов по содержанию основных составляющих
|
Условное обозначение |
Содержание базовых составляющих, % |
Тип флюса |
|
MS |
MnO + SiO2 > 50 |
Марганцево-силикатный |
|
CS |
CaO + MgO + SiO2 > 60 |
Кальцево-силикатный |
|
AR |
Al2O3 + TiO2 > 45 |
Глиноземно-рутиловый |
|
AB |
Al2O3 + CaO + MgO > 45 |
Глиноземно-основный |
|
FB |
CaO + MgO + MnO + CaF2 > 50 |
Фторидно-основный |
|
ST/легирующий |
Нет данных |
Специальный |
Для оценки металлургических
свойств кремнемарганцовистых сварочных флюсов в работе [13] предложена так
называемая «относительная химическая активность» или «относительная активность
по Si и Mn» Аф:
![]() ; (4.19)
; (4.19)
где B – коэффициент основности, SiO2, TiO2 и т.д. –
процентное содержание во флюсе соответствующих компонентов.
В зависимости от коэффициента
активности флюса Аф флюсы можно классифицировать на четыре группы:
-
высокоактивные
(Аф > 0,6);
-
активные (Аф =
0,6 ¸ 0,3);
-
малоактивные (Аф
= 0,3 ¸ 0,1);
-
пассивные (Аф < 0,1).
Коэффициент относительной химической
активности флюса достаточно полно для практических целей характеризует
окислительную способность флюсов (см. рис. 47). Окисление металла шлаком
происходит в результате окислительно-восстановительных процессов, протекающих
на поверхности раздела фаз шлак-металл. Окисление металла приводит к снижению
его пластических свойств, прежде всего, ударной вязкости. На рис. 48 показаны
предельные значения коэффициента химической активности флюса в зависимости от
эквивалента углерода сварочной проволоки для сохранения уровня ударной вязкости
КСU+20 ³ 100 Дж/см2.
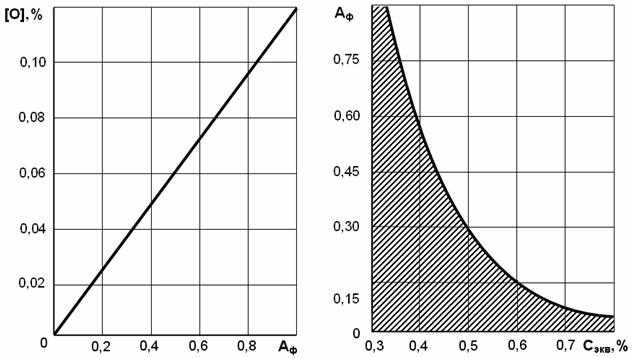
|
Рис. 47. Содержание кислорода в наплавленном металле в зависимости от
величины Аф при сварке углеродистых
и низколегированных сталей |
|
Рис. 48. Зависимость допустимой величины Аф от уровня легирования сварочной проволоки (рекомендуемая
область заштрихована) |
Эквивалент углерода в этом
случае определялся по уравнению (4.20):
![]() . (4.20)
. (4.20)
Активные флюсы (Аф = 0,6 ¸ 0,3) используются для сварки сталей с пределом прочности
sВ £ 600 МПа. Применение их при сварке низколегированных
теплоустойчивых сталей и сталей повышенной и высокой прочности приводит к
загрязнению металла швов неметаллическими включениями, серой и фосфором.
Возможно образование кристаллизационных трещин в металле швов, понижается
стойкость швов против перехода в хрупкое состояние. Для сварки
низколегированных сталей рекомендуются малоактивные флюсы (Аф = 0,3 ¸ 0,1), а для средне- и высоколегированных сталей –
малоактивные и пассивные (Аф < 0,1) флюсы.
По сложившейся в
отечественной практике традиции марка флюса - это обычно наименование
организации – разработчика и порядковый номер флюса. Буквы АН указывают, что
флюс разработан Институтом электросварки им. Е.О. Патона, который функционирует
при Академии наук (АН) Украинской республики. Буква Ц в маркировках флюса ФЦ,
ОСЦ указывает на другого разработчика – ЦНИИТМАШ, г. Москва.
Были попытки связать
маркировку флюса с его металлургическими характеристиками. Например, ОФ-6,
ОФ-10 – основные флюсы; КФ-16 – кислый флюс; НФ-17 – нейтральный флюс. Но эта
практика до сих пор не получила распространения среди разработчиков флюсов.
За рубежом для обозначения
сварочных и металлургических характеристик получила распространение
определенная унифицированная система символов.
Пример: флюс 10saz467.
Первая цифра 10 означает
максимальный ток в сотнях ампер, т.е. в настоящем случае это 1000А.
S – означает, что флюс для
скоростной сварки (Vсв > 60 м/ч). В противном случае S не
ставится.
а – флюс допускает
применение переменного тока, а при сварке на постоянном токе ставится буква в.
Буквы x, y, z означают требуемое напряжение холостого хода
источника питания: X – Uxx £ 65 B; Y – Uxx =
65 ¸ 80 B; Z – Uxx > 80 B.
Последние три цифры
означают химическую активность флюса по углероду, марганцу и кремнию.
Если коэффициент до 4, то
происходит окисление элементов, 5 – флюс нейтрален, от 6 до 9 – прирост
элементов.
ДАЛЕЕ: 4.4. Окисление металла при сварке