Раздел IV.
МЕТАЛЛУРГИЧЕСКИЕ ОСНОВЫ СВАРКИ ПЛАВЛЕНИЕМ
НАЗАД:
4.1. Общая характеристика процессов
в зоне плавления
4.2. Газовая фаза при сварке плавлением
4.2.1. Пути насыщения металла газом при сварке
В результате взаимодействия
с газовой фазой механические свойства металла ухудшаются. Так, сварные
соединения, выполненные в космосе (т.е. в вакууме) имеют механические свойства
на 30 ¸ 40 % выше, чем
аналогичные соединения, выполненные тем же способом сварки в земных условиях.
Более высокие механические свойства имеет и металл, подвергнутый
электрошлаковому переплаву (ЭШП), в процессе которого отсутствует
взаимодействие металла с газовой фазой. Так, у стали марок 20К после ЭШП
снизилась температура хладноломкости с –10 0С до –40 0С.
Для взаимодействия металла
с газом не надо много времени. На воздухе за время 10-7 с
поверхность металла покрывается слоем адсорбированных газов, которые
препятствуют получению качественного сварного соединения.
Источниками газовой фазы
являются:
·
воздух (при
сварке голым электродом в составе газовой фазы его до 75 %, при сварке в
защитных газах – до 5 % за счет подсоса);
·
продукты
диссоциации газообразующих компонентов электродного покрытия или шихты
порошковой проволоки (CaCO3, MgCO3, Cn(H2O)m) – CO2, H2, CO;
·
пары воды;
·
продукты
металлургических процессов – CO, SiF4 TiF4, SiF, TiF, HF, SO2;
·
продукты возгонки
различных элементов;
·
пары металлов,
компонентов электродных покрытий, флюсов, шихты порошковой проволоки (давление
этих паров может составлять 0,15 ¸ 0,25 атм);
·
защитные газы (CO2, Ar, He, газовые
смеси).
·
По характеру
газовая фаза может быть:
·
нейтральная (например,
Ar и He);
·
окислительная (CO2, O2, H2О);
·
восстановительная
(СО, Н2).
Насыщение металла газами
происходит несколькими путями. Основной путь – это химическое поглощение
(растворение). Количество растворенного в металле газа “r” определяется уравнением Генри
[Cr] = kPr; (4.1)
или законом Сиверса
[Cr] = k1Pr + k2![]() ; (4.2)
; (4.2)
где К, К1, и К2 – постоянные величины,
зависящие от температуры, свойств газа и металла;
Pr
и Pr2 – парциальные давления атомарного и молекулярного
газа «r».
В основном растворяются
атомарные газы. Молекулярным газам должна предшествовать их диссоциация на
атомы. Так, растворимость атомарного азота в е18 раз выше, чем
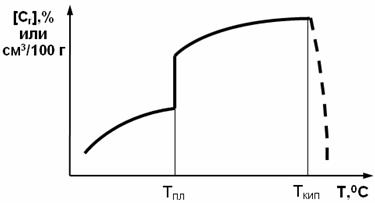
молекулярного. Температурная зависимость растворимости газов схематично
представлена на рис. 40,а. Насыщение газом происходит в основном при жидком
состоянии металла, но титан, например, начинает интенсивно поглощать газы с
температуры выше 350 0С. Наиболее интенсивно насыщение газами
происходит на стадии капли, этому способствует высокая температура, близкая к
температуре кипения, и большая относительная поверхность капли.
Максимальная
растворимость газов в железе
Газ
|
20 0С |
1500 0С |
2500 0С |
Кислород,%
|
0,035 |
0,16 (0,22) |
2 |
Азот,%
|
0,001 |
0,04 |
0,06 |
Водород, см3/100г
|
10-3 |
25 |
42 |
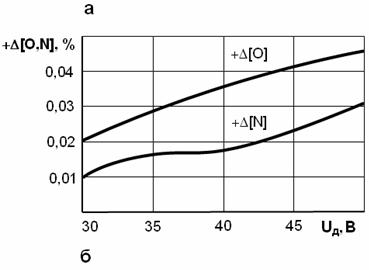
Рис.40. Растворимость газов
в металле:
а – характер химического растворения; б –
электрическое растворение кислорода и
азота в сталях
В дуге наблюдается и электрическое
поглощение газов на катоде. Положительные ионы под действием электрического
поля бомбардируют поверхность катода, нейтрализуются и диффундируют вглубь
металла. Электрическая растворимость зависит от газа, режима сварки (катодного
падения напряжения), наличия третьих компонентов, окисных пленок. На рис. 40,б
представлена зависимость электрического поглощения кислорода и азота в
зависимости от напряжения дуги. Из графика видно, что для уменьшения содержания
газов в металле шва сварку надо вести короткой дугой.
Кроме того,
насыщение металла газами может происходить в результате хемосорбции. Процесс
протекает следующим образом: вначале осуществляется адсорбция (поверхностное
поглощение) газа, затем на поверхности металла образуются химические соединения
(происходит хемосорбция), которые диффундируют вглубь металла.
Итак, металл всегда
содержит какое-то количество газов в виде отдельных включений (газовых
включений или пор), химических соединений или твердого раствора. В твердом
металле лишь до 10 % азота и кислорода находятся в растворенном состоянии,
остальной газ в виде оксидов и нитридов, расположенных в виде межзеренных или
межкристаллитных прослоек.
ДАЛЕЕ:
4.2.2. Влияние кислорода на
свойства металла