Глава 3 СТРОЕНИЕ И СВОЙСТВА МЕТАЛЛОВ
Назад: 3.2 Дефекты кристаллической решетки
металлов.
3.3 Диаграммы состояния металлических
сплавов
Процессы
кристаллизации металлических сплавов и связанные с ними закономерности образования
структуры описывают, как известно [1], с помощью диаграмм состояния или
диаграмм фазового равновесия. Диаграмма
состояния – это графическое изображение фазового или структурного состава всех
сплавов данной системы, находящихся в равновесном (неизменном) состоянии при данной
температуре и концентрации компонентов. Обычно их строят для двойных, реже
тройных и многокомпонентных систем сплавов. С помощью диаграмм состояния
определяют температуры плавления и кристаллизации сплавов, полиморфных и других
превращений в сплавах, природу фаз и их количественное соотношение в системе,
что позволяет судить о механических и технологических свойствах сплавов.
Диаграммы состояния строят для условий равновесия или достаточно близких к ним,
т.е. при весьма малых скоростях нагрева и охлаждения сплавов.
В
большинстве случаев сплавы находятся в метастабильном состоянии, т.е. в таком,
когда они обладают ограниченной устойчивостью в данных условиях и под влиянием
внешних воздействий (например, нагрева) переходят в более устойчивые состояния
с минимумом свободной энергии системы (например, переход металла в жидкое
состояние при нагреве).
Диаграммы
состояния сплавов различаются в зависимости от степени взаимной растворимости
компонентов, способности образовывать твердые растворы, химические соединения
или претерпевать полиморфные превращения. Подробный их анализ приведен в
работе. [3]
Представляет
особый интерес диаграмма состояния сплава, один из компонентов которого
обладает полиморфными превращениями, вызывающими скачкообразное изменение
растворимости другого компонента в твердом состоянии. Примером такого сплава,
имеющего большое практическое значение, является сплав железа с углеродом (рис.
3.8) .
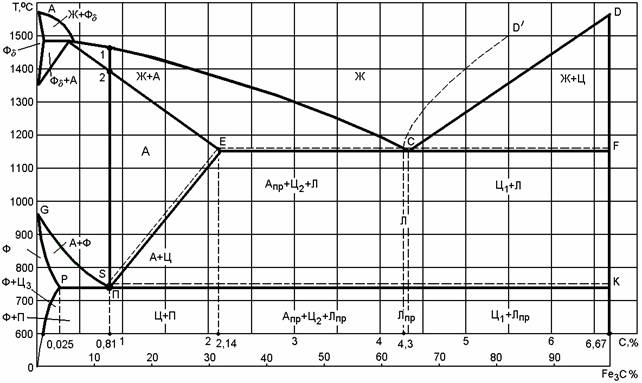
Рис. 3.8 –
Диаграмма состояния сплава железо-углерод (цементит)
Основным
компонентом сплава железо-углерод (железо-цементит) является железо. В твердом состоянии
оно имеет две полиморфные модификации – ![]() и
и ![]() . Модификация Fe
. Модификация Fe![]() (ОЦК) устойчива при температурах ниже 910 0С и
выше 1392 0С. Высокотемпературную модификацию
(ОЦК) устойчива при температурах ниже 910 0С и
выше 1392 0С. Высокотемпературную модификацию ![]() -железа нередко обозначают как Fe
-железа нередко обозначают как Fe![]() . Модификация Fe
. Модификация Fe![]() (ГЦК) существует при температурах 910...1392 0С.
Критическую температуру
(ГЦК) существует при температурах 910...1392 0С.
Критическую температуру ![]() превращения при
нагреве обозначают Ас3, а при охлаждении Аr3. Критическую
температуру
превращения при
нагреве обозначают Ас3, а при охлаждении Аr3. Критическую
температуру ![]() превращения при Т=1392
0С обозначают АС4(Аr4). Температура магнитного
превращения обозначается как Ас2.
превращения при Т=1392
0С обозначают АС4(Аr4). Температура магнитного
превращения обозначается как Ас2.
Другим
компонентом системы является углерод. В зависимости от содержания углерода и температуры
в сплаве железо-углерод наблюдаются как однофазные структурные образования –
жидкий раствор углерода в железе, твердые растворы углерода в железе – феррит и
аустенит, химическое соединение железа с углеродом – цементит, так и двухфазные
структурные составляющие – перлит и ледебурит. Их состав, характеристики и
свойства изучались в курсе «Материаловедение» и подробно изложен в литературе
[1], а сокращенные названия фаз обозначены на диаграмме (рис. 3.8).
Диаграмму Fe-C
можно разделить на две части вертикальной линией, проходящей через точку Е.
Сплавы, расположенные слева от точки Е, характеризуются тем, что при
затвердевании от точки плавления образуют структуру твердого раствора углерода
в ![]() -железе, т.е. аустенита. Эти сплавы называются сталями.
Справа от точки Е кристаллизация сплава заканчивается образованием эвтектики,
называемой ледебуритом. Это область чугунов.
-железе, т.е. аустенита. Эти сплавы называются сталями.
Справа от точки Е кристаллизация сплава заканчивается образованием эвтектики,
называемой ледебуритом. Это область чугунов.
Фазовые
превращения в стали при охлаждении удобнее рассматривать с точки, в которой содержится
углерода 0,81 %, т.е. по вертикали 1-2-S-0,81. В интервале температур от точки
1 до точки 2 сплав будет двухфазным: жидкость + аустенит. При дальнейшем охлаждении от точки 2 до точки S отмечается
область устойчивого существования аустенита, а в точке S происходит распад
аустенита с образованием вторичного цементита:
Fe![]() ( C)
( C) ![]() Fe
Fe![]() ( C) + Fe3C.
( C) + Fe3C.
Продуктом
распада является феррито-цементитная смесь, содержащая 0,81 % углерода и названное
перлитом, само превращение называется эвтектоидным, а сталь – перлитной.
Температура эвтектоидного превращения обозначается как Ас1. Процесс
кристаллизации и превращения в сталях, содержащих больше или меньше 0,81 %
углерода идет аналогично (по линиям SE и SG). В связи с этим стали делят на
доэвтектоидные (С < 0,8 %), эвтектоидные (С = 0,8 %) и заэвтектоидные (С
> 0,8 %), а чугуны соответственно делятся на доэвтектические (С < 4,3 %),
эвтектические (С = 4,3 %) и заэвтектические (С > 4,3 %).
Как
видно из рис. 3.8, структура большинства доэвтектоидных сталей после медленного
охлаждения состоит из двух фаз – феррита и перлита. С увеличением количества
углерода уменьшается количество феррита и возрастает количество перлита т.е.
фактически растет количество цементита. Твердые и хрупкие частицы цементита повышают
сопротивление движению дислокаций, т.е. повышают сопротивление деформации и,
кроме этого, уменьшают пластичность и вязкость. В частности, отмечается [3], что каждые
0,1 % С повышает температуру порога хладноломкости Ткр в среднем на
20 % и расширяют интервал перехода от вязкого к хрупкому разрушению. Углерод также
оказывает существенное влияние на технологические свойства стали:
свариваемость, обрабатываемость давлением, резанием, о чем будет подробнее
указано ниже.
Учитывая,
что любая сталь является многокомпонентным сплавом, содержащим кроме углерода и
ряд других элементов (Mn, Si, S, P), кратко обозначим влияние этих элементов на
свойства сплава.
Кремний
и марганец, содержащиеся в качестве компонентов (Mn ![]() 0,5...0,8 %, Si
0,5...0,8 %, Si ![]() 0,35...0,4 %),
переходящих в сталь в процессе раскисления, упрочняют феррит, несколько снижая
пластичность, а марганец, понижает красноломкость стали.
0,35...0,4 %),
переходящих в сталь в процессе раскисления, упрочняют феррит, несколько снижая
пластичность, а марганец, понижает красноломкость стали.
Сера
образует эвтектику (Fe+FeS) с Тпл = 988 0С, которая,
расплавляясь при прокатке, ковке (Т = 1000...1200 0С) и сварке
нарушает связь между зернами и способствует образованию надрывов и трещин
(красноломкость). Одновременно сера снижает ![]() –1,
–1, ![]() , свариваемость и коррозионную стойкость. Ее содержание
ограничивается в пределах 0,03...0,06 %.
, свариваемость и коррозионную стойкость. Ее содержание
ограничивается в пределах 0,03...0,06 %.
Фосфор,
повышает жидкотекучесть, но охрупчивает сталь и уменьшает пластичность и вязкость.
Его содержание ограничивается в пределах 0,025...0,08 %.
Азот,
кислород и водород присутствуют в стали как в газообразном виде (в раковинах,
порах, микротрещинах и т.п.), так и в виде твердых растворов внедрения и хрупких
неметаллических включений FeO, SiO2, Fe2N, Al2O3
и т.д. Неметаллические включения, располагаясь по границам зерен, снижают
ударную вязкость и предел выносливости стали. Водород, накапливаясь в
микропустотах, вызывает появление пор и часто способствует образованию
«замедленных» трещин.
В
условиях неравновесного (ускоренного) охлаждения, характерного для процессов
сварки, ковки, прокатки, как правило, образуются пересыщенные твердые растворы
углерода, кислорода и азота в железе. Постепенное выделение O2 и N2
из пересыщенных растворов при нормальной или повышенной рабочей температурах
приводит к изменению свойств сталей. Этот процесс называется термическим
старением. Как правило, оно повышает прочность стали и снижает ударную
вязкость, повышая порог хладноломкости. Старение возможно и после холодной пластической
деформации (если она проводится ниже температуры рекристаллизации). Такой
процесс называется деформационным старением.
Таким
образом, диаграмма состояния сплавов железо-углерод позволяет качественно
оценить изменения структуры и свойств стали при технологических воздействиях,
связанных с нагревом, охлаждением или деформацией.
Далее: глава 4 ЛЕГИРОВАНИЕ
ЖЕЛЕЗОУГЛЕРОДИСТЫХ СПЛАВОВ И ИХ СВАРИВАЕМОСТЬ